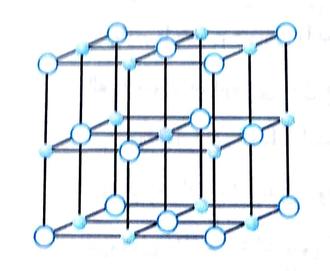
تغییر آنتالپی مربوط به تراکم یون های مثبت
و منفی برای یک شبکه بلوری را انرژی شبکه گویند. از عوامل موثر بر انرژی شبکه می توان گفت: 1- بار2- شعاع یونها3-
نوع شبکه
منیزیم اکسید مانند سدیم کلرید است یعنی مکعب مراکز وجوه پر
و آلومینیوم اکسید در شکل آلفا دارای شبکه ی اچ سی پی از یونهای اکسید است که دو سوم
حفره های هشت وجهی به وسیله کاتیون ها اشغال شده اند.با وجود اینکه انرژی شبکه
آلومینیم اکسید بیشتر از منیزیم اکسید است ولی چون شبکه بلور منیزیم اکسید متراکم
تر است نقطه ذوب آن بیشتر از آلومینیم اکسید است.
مقایسه انرژی شبکه پتاسیم فلورید و سدیم برمید برای دانش
آموزان کار ساده ای نیست. در این مورد چون بار یونها برابر است اگر دانش آموز شعاع
یونها را داشته باشد می تواند با جمع شعاع یونی در یابد که کدام شبکه چگالی بار
بالاتری دارد. به طور مثال در این مورد با توجه به این که شعاع فلوئور پایین است
دریابد که انرژی شبکه آن بیشتر است.
در غالب مواقع اثر بار بیشتر از شعاع است اما موارد استثنا
هم وجود دارد
انرژی شبکه Ca3N2کمتر از CaF2 هست. بار آنیونNاز آنیون Fبیشتر است اما شعاعش هم بیشتراست . در اینجا عامل دیگری در
انرژی شبکه موثر است. هر چه چگالی بار بیشتر باشد انرژی شبکه بلور بیشتر است بار به حجم مساوی چگالی بار را بدست می دهد. در
اینجا اندازه یون نیترید خیلی بزرگتر از یون فلوئورید است و شبکه بلور کلسیم کلرید هم انباشته تر باشد
در مورد کلسیم نیترید یکی از دلایل کمتر بودن انرژی شبکه اینست
که قطبش پذیری یون نیترید زیاد است و پیوند کمی کوالانسی می شود وکاملا جاذبه یونی
قوی نیست ونقطه ذوب کمتر می شود.
کلسیم نیترید بعلت بزرگ
بودن یون نیترید نمی تواند بلور با این فشردگی کلسیم فلوئورید بسازد
چگالی کلسیم نیترید 2.67 و چگالی کلسیم فلویورید 3.18 است. نقطه
ذوب کلسیم نیترید1195 و کلسیم فلویورید2533 است.
معمولا انرژی شبکه با دمای ذوب و جوش هماهنگ است اما گاهی
مشاهده می شود که این دو هماهنگ عمل نمی کنند به طور مثال انرژی شبکه آلومینیوم
اکسید بیش تر از منیزیوم اکسید است اما دمای ذوب منیزیوم اکسید بالاتر است. برای
توجیه این پدیده دو عامل را می توان بیان کرد.
1- می توان گفت در الومینیم اکسید قطبش
پذیری یون اکسید بوسیله یون الومینیم بیشتر رخ می دهد از قدرت یونی کم شده و خصلت
کووالانسی افزایش می یابد و نقطه ذوب کمتر می شود.
پاولینگ معتقد بوده
که دمای ذوب هالیدهای لیتیم با انچه پیش بینی می شده هماهنگ نیست و معتقد بوده که لیتیم
یون کوچکی است(همانند الومینیوم ) و به دلیل چگالی بالا یونهای هالید را پلاریزه می
کند و در واقع پیوندها کووالانسی می شوند و به طور کامل یونی نیستند.
2- اما عامل دوم موثر بیان شده این
است که وقتی یون های مثبت و منفی کنار هم قرار میگیرند به دلیل شعاع کوچک کاتیون
یون های منفی به هم نزدیک شده و بر هم دافعه وارد می کنند و این باعث کاهش دمای
ذوب می شود.
در اینجا سه عامل درگیر است ۱- بار یون ها یکی نیست ۲- اندازه
یونها یکی نیست ۳-شبکه بلور یکی نیست پس نمی
توان گفت این سه عامل همسو هستند.
در مبحث تعیین انرژی شبکه، مثالهای دیگری هم هست که دوعامل بار
و شعاع یون هماهنگ عمل نمی کنند. پس ما نمیتونیم پیش بینی دقیقی داشته باشیم و فقط
می توانیم درصورت آگاهی از کمتر یا بیشتر بودن مقدار انرژی شبکه، آن را توجیه کنیم.